合成微/納馬達是一種微型化裝置,可以通過轉(zhuǎn)換外部能量或化學燃料轉(zhuǎn)化為自主運動,用于靶向給藥、體內(nèi)成像和微創(chuàng)手術(shù)等。中山大學材料科學與工程學院彭飛副教授團隊提出,還可以將微納米馬達作為一種與神經(jīng)系統(tǒng)通信的新方式。
通過鎳-鋅(Ni-Zn)微馬達信號傳導(dǎo)誘導(dǎo)神經(jīng)干細胞定向分化
神經(jīng)干細胞具有自我更新、分化和環(huán)境調(diào)節(jié)的能力,被認為在中風、腦損傷治療和神經(jīng)元再生方面很有前景。內(nèi)源性神經(jīng)干細胞的激活,吸引著越來越多的研究熱情,避免了免疫排斥和外源性細胞移植的倫理問題。然而,如何在原位誘導(dǎo)定向生長和分化仍然是一個主要的挑戰(zhàn)。
近期,彭飛副教授團隊提出了一種基于自建立的電化學場的非侵入性純水驅(qū)動的Ni-Zn微馬達(圖1a)。在Zn端,H?被還原生成H?和Zn2?。Zn2?的逐漸積累產(chǎn)生了濃度梯度和驅(qū)動Ni-Zn微馬達的自構(gòu)造電場。有趣的是,與以前的化學驅(qū)動微馬達相比,Ni-Zn微馬達在運動過程中沒有產(chǎn)生氣泡,從而避免了氣體栓塞。
微馬達可以磁引導(dǎo)和精確接近目標神經(jīng)干細胞,在定位和可控性方面具有獨特的優(yōu)勢。水驅(qū)動的Ni-Zn微馬達在運動過程中產(chǎn)生Zn2?。Zn2?場和電壓門控Ca2?通道的激活,導(dǎo)致細胞內(nèi)Ca2?的短暫變化,從而激活后期神經(jīng)干細胞的分化。接近電池后,由于馬達自身Zn端到Ni端的濃度梯度,在單個馬達上形成自構(gòu)造的電場。
神經(jīng)干細胞受到Ni-Zn微馬達電場的影響,產(chǎn)生生物電信號,這是誘導(dǎo)神經(jīng)干細胞分化的一個因素。Zn2?還具有促進干細胞增殖、神經(jīng)發(fā)生和神經(jīng)元分化的作用。因此,我們有理由認為,微馬達釋放的Zn2?對維持神經(jīng)干細胞中的Zn2?穩(wěn)態(tài)具有重要意義。
因此,微馬達通過電化學場,允許生物電信號與內(nèi)源性神經(jīng)干細胞進行交換和通訊,從而允許在體內(nèi)調(diào)節(jié)神經(jīng)元增殖和定向分化(圖1b)。因此,該研究開發(fā)了一種結(jié)合電和化學效應(yīng)的非侵入性和持久的神經(jīng)刺激系統(tǒng)。它使與神經(jīng)干細胞再生和分化相關(guān)的信號通路能夠得到持久的激活。有針對性和持久的效果,同時避免嚴重的術(shù)后創(chuàng)傷和并發(fā)癥。
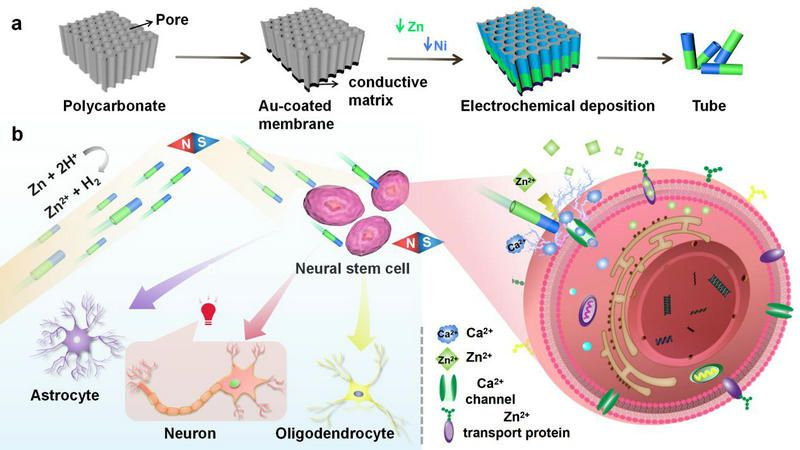
圖1 Ni-Zn微馬達的制備及靶向激活神經(jīng)干細胞和引導(dǎo)細胞分化的示意圖
該工作以“Directed Neural Stem Cells Differentiation via Signal Communication with Ni-Zn Micromotors”為題,發(fā)表在Advanced Materials期刊上。中山大學材料科學與工程學院2021級博士研究生封燁為獨立第一作者,中山大學材料科學與工程學院彭飛副教授為通訊作者。
納米機器人介導(dǎo)的同步神經(jīng)元激活
在自然界中,從細菌菌落到魚群,再到哺乳動物群體,生物可以聚集在一起形成群體并呈現(xiàn)大規(guī)模的集體行為。這些集體群體的例子很有吸引力,獨立的個體群體通過通信構(gòu)建了比自己大幾個數(shù)量級的復(fù)雜結(jié)構(gòu)。這種信息交換可以表現(xiàn)為包括振蕩在內(nèi)的群體模式。操縱神經(jīng)元振蕩和探索信息交換是非常有趣的,這可以為腦科學、人工智能和機器人技術(shù)提供啟示。但當下人工設(shè)計合成交互系統(tǒng)仍然是一個挑戰(zhàn)。
近期,彭飛副教授團隊提出了振蕩納米機器人的程序化集群,其推進和集群背后的場信息作為體外與生物神經(jīng)元通信并觸發(fā)神經(jīng)振蕩的介質(zhì)。如圖2a所示,該研究設(shè)計了一個由近紅外光驅(qū)動的高度可控的振蕩納米機器人群。納米機器人通過純水的光催化分解驅(qū)動電泳(并自建立的化學-電場梯度)。
通過程序化的近紅外光照射,納米機器人群呈現(xiàn)周期性化學-電場和集體動態(tài)可逆收縮-膨脹-收縮(振蕩)行為。局部視網(wǎng)膜神經(jīng)節(jié)細胞(RGC)可以通過來自集群的振蕩電場有節(jié)奏地激活。神經(jīng)元與編程的納米機器人集群節(jié)奏同步。有趣的是,在通過耦合振蕩使沒有物理接觸的神經(jīng)元群中觀察到同步周期性的波紋活動,類似于自然神經(jīng)系統(tǒng)中的振蕩網(wǎng)絡(luò)(圖2b)。
共振允許原本無法到達毫米級外的神經(jīng)元信號得以傳輸,這不同于神經(jīng)元通常認為需要突觸直接連接和同步的方式。與數(shù)量有限的孤立神經(jīng)元相比,神經(jīng)元共振具有重要意義,因為大量同步神經(jīng)元群誘導(dǎo)下游神經(jīng)反應(yīng)的機會更高。節(jié)律神經(jīng)活動還允許在不同時間窗口(即節(jié)律周期的特定階段)進行神經(jīng)興奮性調(diào)節(jié),以便神經(jīng)元組可以通過鎖相神經(jīng)振蕩精確地相互作用。這代表該合成可編程振蕩平臺提供了與神經(jīng)元系統(tǒng)通信的新方式。
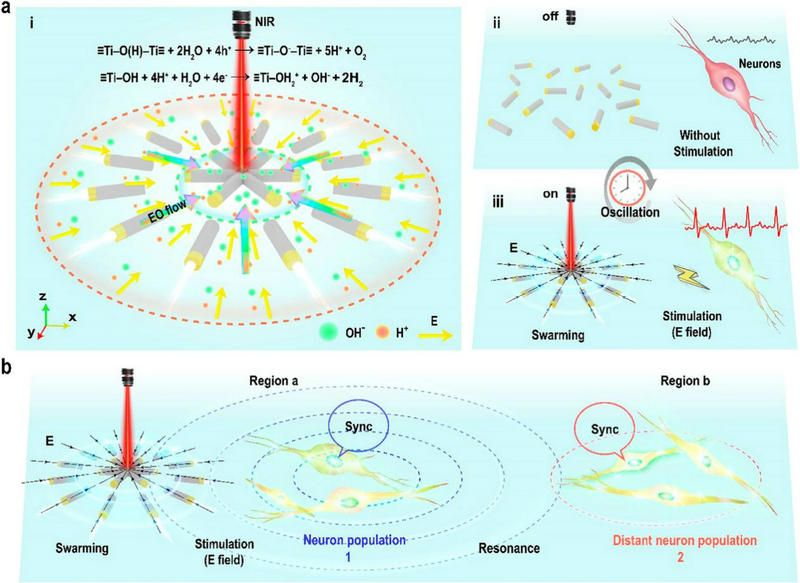
圖2 編序化近紅外下的振蕩納米機器人集群和不同區(qū)域神經(jīng)元群的同步周期性漣漪的示意圖
該工作題以“Nanorobot-Mediated Synchronized Neuron Activation”為題,發(fā)表在ACS Nano期刊上。中山大學材料科學與工程學院2022級博士研究生陳彬為獨立第一作者,中山大學材料科學與工程學院彭飛副教授為通訊作者。相關(guān)工作得到國家自然科學基金資助項目,廣東省杰出青年科學基金項目,國家重點研發(fā)計劃項目的支持。
審核編輯:劉清
-
驅(qū)動器
+關(guān)注
關(guān)注
54文章
8652瀏覽量
149452 -
振蕩器
+關(guān)注
關(guān)注
28文章
3979瀏覽量
140621 -
人工智能
+關(guān)注
關(guān)注
1805文章
48890瀏覽量
247797 -
RGC
+關(guān)注
關(guān)注
0文章
2瀏覽量
6040 -
納米機器人
+關(guān)注
關(guān)注
0文章
43瀏覽量
11851
原文標題:中山大學在微納馬達用于神經(jīng)調(diào)控方面取得新進展
文章出處:【微信號:MEMSensor,微信公眾號:MEMS】歡迎添加關(guān)注!文章轉(zhuǎn)載請注明出處。
發(fā)布評論請先 登錄
洲明數(shù)字文化科技與中山大學旅游學院達成戰(zhàn)略合作
紫光同創(chuàng)攜手中山大學助力集成電路產(chǎn)業(yè)創(chuàng)新人才培養(yǎng)
神經(jīng)網(wǎng)絡(luò)RAS在異步電機轉(zhuǎn)速估計中的仿真研究
上海光機所在強場太赫茲對砷化鎵偶次諧波調(diào)控研究方面取得新進展
會議回顧:Aigtek亮相2025微納技術(shù)應(yīng)用創(chuàng)新大會,助力開啟微納未來科技大門!

量子計算+醫(yī)療 玻色量子與中山大學附屬第三醫(yī)院達成戰(zhàn)略合作
睿創(chuàng)微納短波紅外探測器助力超新星觀測
微電網(wǎng)協(xié)調(diào)控制器:構(gòu)建未來能源互聯(lián)網(wǎng)的神經(jīng)中樞

中山大學:在柔性觸覺傳感電子皮膚研究進展
聚焦AI語音!聲揚科技張偉彬博士受邀為中山大學深圳校區(qū)師生作分享

中山大學最新發(fā)布:27.30%效率背接觸BC電池的創(chuàng)新表征技術(shù)

千呼萬喚始出來!中山大學-創(chuàng)龍教儀RK3568教學實驗室項目正式落地!

鄭州大學在鈣鈦礦量子點閃爍體研究方面取得重要進展





 中山大學在微納馬達用于神經(jīng)調(diào)控方面取得重大研究
中山大學在微納馬達用于神經(jīng)調(diào)控方面取得重大研究











評論