本文總結(jié)回顧了鋰電電極的熵變和塞貝克系數(shù)(Seebeck coefficient)的檢測,并展示了如何通過塞貝克系數(shù)計算電極的帕爾貼熱(Peltier heat)。塞貝克系數(shù)取決于傳遞熱(Soret effect),該熱是通過塞貝克系數(shù)的初始狀態(tài)值和穩(wěn)態(tài)值之差得出的。
此外,應(yīng)用非平衡熱力學理論獲得了以前未報道的帕爾貼熱。對于鋰金屬的氧化,當電解質(zhì)為1 M LiPF6 時,得出帕爾貼熱為34±2 kJ mol-1,當電解質(zhì)為1 M LiClO4 時,帕爾貼熱為29±1 kJ mol-1。正值表示陽極溫度降低。
對于在穩(wěn)態(tài)條件下的鋰氧化,珀耳帖熱為120kJ mol-1,遠大于全電池的熵變,顯示對單極產(chǎn)生較大的可逆加熱效果。最后,指出了測量可逆熱效應(yīng)在電池中的重要作用以及其在未來的機遇。
【內(nèi)容詳情】在儲能方面,鋰離子電池(LIB)已成為世界領(lǐng)先的電池技術(shù)之一。其電極包含插層的鋰、電解質(zhì)通常由兩種或更多種有機成分(溶劑)和鋰鹽組成。鋰電池已被廣泛應(yīng)用于小型電子設(shè)備、電動汽車,甚至輪船和渡輪中的大型電池組。這些新應(yīng)用對電池的使用壽命、容量和安全性提出了新的要求。
眾所周知,溫度對鋰電的性能起著重要作用。因此,數(shù)十年來熱模型和老化模型一直是人們關(guān)注的話題。準確的熱模型有助于理解和控制老化機制。單電池熱建模的準確性對于大型電池組的建模也非常重要。
鋰電的熵變來自電極反應(yīng)和電解質(zhì)中的電荷轉(zhuǎn)移。在圖1為全電池和半電池的示意圖。與熱模型中的不可逆效應(yīng)相比,在中等和高充電/放電倍率下,電極可逆熱效應(yīng)可以忽略。但是,最近出現(xiàn)了一個新的協(xié)議,即在所有熱模型中都需要包括可逆熱效應(yīng)。
但是,對于鋰電來說,最常見的做法是包括電池的總可逆熱效應(yīng)或反應(yīng)的熵變。總效果已均勻分布在整個單元上。但是,由于電極的位置不同,因此電極表面的局部熱效應(yīng)可能與平均總效應(yīng)不同。
盡管總熱效應(yīng)為局部效應(yīng)的總和,但局部熱效應(yīng)并不一定是均勻的,每個局部效應(yīng)可以大于或小于總效果,甚至可以具有不同的正負值,產(chǎn)生局部冷熱效應(yīng)。從非平衡熱力學的角度來說,局部可逆效應(yīng)確實比電池的可逆熱效應(yīng)的總和大得多。因此,在高充電/放電倍率下,可逆熱效應(yīng)在電池建模中起著更加重要的作用。
【全電池和半電池熵變的測量】根據(jù)經(jīng)典熱力學,電化學電池的熵與電動勢和溫度有關(guān),等式(1):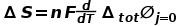 其中n是參與電極反應(yīng)的電子數(shù),F(xiàn)是法拉第常數(shù),T是等溫電池的溫度,
其中n是參與電極反應(yīng)的電子數(shù),F(xiàn)是法拉第常數(shù),T是等溫電池的溫度,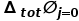 是電池電流為0時的電動勢,即開路電壓E。等式(1)適用于全電池和半電池。
是電池電流為0時的電動勢,即開路電壓E。等式(1)適用于全電池和半電池。
熵變與可逆熱的關(guān)系如下,等式(2):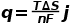 其中q是電池中每單位時間所產(chǎn)生的總可逆熱量。在非平衡熱力學中,電極表面的局部熵平衡通過珀耳帖熱計算。
其中q是電池中每單位時間所產(chǎn)生的總可逆熱量。在非平衡熱力學中,電極表面的局部熵平衡通過珀耳帖熱計算。
總的可逆熱效應(yīng),即具有陰陽電極全電池的熵變,可通過等式(1)獲得。據(jù)報道,可以根據(jù)半電池的熵變來估計全電池熵變。典型的實驗步驟是,使用水浴或恒溫槽,對電池進行保溫,并通過熱電偶來控制溫度。通過測試特定溫度下的電動勢即可獲得全電池的熵變,詳情請參考(Phys. Chem. Chem. Phys., 2017, 19, 9833-9842)
全電池的熵變也可以通過單個電極的珀耳帖熱獲得。需要注意的是,對于單個電極珀耳帖熱量,需要在相同電解質(zhì)中測的。必須注意的是,半電池的熵變并不等于單個電極表面的局部熱效應(yīng)。這是文獻中常見的誤解。
原因是局部熱效應(yīng)(珀耳帖熱)包含其他熱效應(yīng),包含但不限于半電池電極的熵變。例如,Wittingham首次通過使用嵌入度為0.6和1的LixTiS2(LTS)電極,報道了半電池的熵變。Dahn和Honders等也研究了LixTiS2的熵變,并獲得與Whittingham一致的結(jié)果。這些結(jié)果有利于進一步的了解電極材料的相圖。
【半電池和珀耳帖熱量測量】對于鋰金屬│電解質(zhì)│電極,陽極反應(yīng)(等式3)為:Li→Li+ + e-與該反應(yīng)相關(guān)的熱量是局部可逆熱效應(yīng),由單電極珀耳帖熱量πs,i給出,其中i = a或c表示陽極或陰極界面,而s表示表面。珀爾帖熱將由界面區(qū)域上的熵獲得(請參見下文)。通過熱的形式增加熵變,必須補償鋰消耗所釋放的熵變,包括電極中的電子轉(zhuǎn)移的熵變以及鋰離子轉(zhuǎn)移到電解質(zhì)中的熵變。
一個普遍的誤解是,單電極的珀耳帖熱可以從半電池的溫度變化中得到,或者可以從圖1b中的半電池的熵變獲得局部熱量的產(chǎn)生。理論證明,電池的熵變通常等于所用電極的單電極珀耳帖熱之差。通過等式(4)獲得:TΔS=πs,a – πs, c
【熱電電池理論】Gunnarshaug等人推導了具有三元電解質(zhì)和兩個相同LiFePO4電極的熱電電池的塞貝克系數(shù)。在圖2所示的測量中,沿垂直于電極表面的方向電池施加溫度差,只需要考慮一維運輸過程。在圖2b給出了熱電電池所使用的相關(guān)符號。
【塞貝克系數(shù)】通過三步可以得出圖2a所示電池的塞貝克系數(shù)的表達式。(1)找到每個單元層或界面的熵產(chǎn)生。(2)確定運輸?shù)谋緲?gòu)方程。(3)將適當?shù)姆匠淌脚c實驗或過程的邊界條件進行積分,以得出電動勢和溫度差之間的關(guān)系。磁通力方程為:
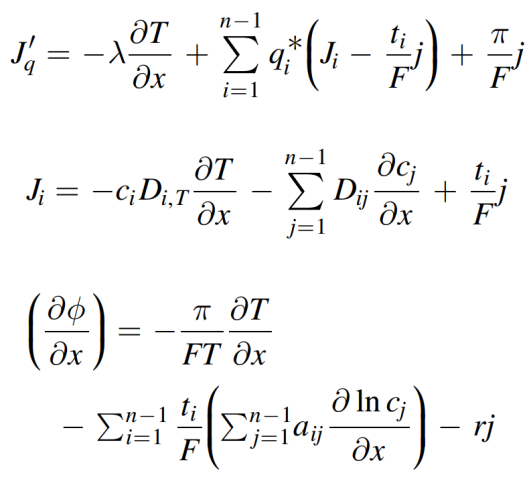
最后一步是每個階段積分的方程式,電勢與熱動勢的關(guān)系,也給出了圖2a中電池每部分的塞貝克系數(shù)的貢獻,包括體相電極、電極反應(yīng)以及電解質(zhì)。因此,可以對每一部分的貢獻進行加和,即可得到總的塞貝克系數(shù)。
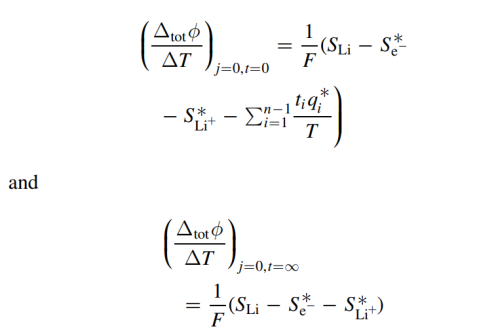
【根據(jù)半電池熵變計算的珀耳帖熱量】通過等式TΔS=πs,a – πs, c可以確定陰極的珀耳帖熱。因此,只需要知道另一個陽極的電池熵和珀爾帖熱,即可獲得全電池的總帕爾貼熱。陰極的珀耳帖熱量為: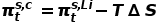 其中ΔS表示電池放電的熵變,
其中ΔS表示電池放電的熵變,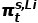 是在任何狀態(tài)t下鋰陽極的珀耳帖熱。此公式適用于穩(wěn)態(tài)和初始狀態(tài)。金屬電極的初始狀態(tài)珀耳帖熱隨電解質(zhì)類型的變化不大。因此,陰極的珀耳帖熱的變化只與電荷狀態(tài)或溫度的變化與ΔS有關(guān)。
是在任何狀態(tài)t下鋰陽極的珀耳帖熱。此公式適用于穩(wěn)態(tài)和初始狀態(tài)。金屬電極的初始狀態(tài)珀耳帖熱隨電解質(zhì)類型的變化不大。因此,陰極的珀耳帖熱的變化只與電荷狀態(tài)或溫度的變化與ΔS有關(guān)。
石墨電極獲得的半電池熵變化以及相應(yīng)的初始狀態(tài)珀耳帖熱,a中的熵變顯示從30-60 J K-1 mol到-20 J K-1 mol,在x≈0.4的熵變最小。該值可以為正也可以為負,具體取決于組成。但是,b中相應(yīng)的珀耳帖熱量始終為正,表示電極表面溫度降低。
【總結(jié)與展望】總之,鋰離子電池中最重要的局部可逆熱效應(yīng)是單電極表面的珀耳帖效應(yīng)。根據(jù)電池的熵變和電極的珀耳帖熱,可以確定另一電極的珀耳帖熱。鋰金屬熱電電池的塞貝克系數(shù)的測量值和半電池熵數(shù)據(jù),已被廣泛用于陽極反應(yīng)的各種成分和鋰化程度的珀耳帖熱計算。
對于鋰電極而言,初始狀態(tài)的珀爾帖熱具有良好的可靠性。但是缺乏鋰電關(guān)于Dufour效應(yīng)的數(shù)據(jù),因此,需要對珀耳帖穩(wěn)態(tài)熱進行更進一步地研究。
此外,非平衡熱力學理論表明,大的可逆熱效應(yīng)相關(guān)的電極,可能反而具有較小的局部熱效應(yīng)。這表明測量電極的珀耳帖熱的重要性,其不僅可以獲得總可逆熱效應(yīng),還可用來獲得新的珀耳帖熱。
對于鋰金屬陽極,電解質(zhì)為1M LiClO4時,其初始帕爾帖熱參考值為34±2 kJ mol-1,而當電解質(zhì)為1M LiPF6時,初始帕爾帖熱參考值為29±2 kJ mol-1。該初始值對有機溶劑不敏感。
陰極的珀耳帖熱同樣不敏感。當電極用作陽極時,對于穩(wěn)態(tài)珀爾帖熱,該值將升高到140 kJ mol-1。這是一個很大的可逆加熱效應(yīng),遠大于全電池熵變化的預期值。研究初始和特定狀態(tài)下的塞貝克系數(shù)和半電池熵變,對電池的系統(tǒng)性研究具有重要意義。關(guān)于Dufour效應(yīng)的研究仍然缺少,例如從穩(wěn)態(tài)和初始狀態(tài)的塞貝克系數(shù)與Dufour效應(yīng)的關(guān)系等。
Astrid F. Gunnarshaug, Preben J. S. Vie, and Signe Kjelstrup*,
Review—Reversible Heat Effects in Cells Relevant for Lithium-Ion Batteries, J. Electrochem. Soc. 2021,168,050522.https://iopscience.iop.org/article/10.1149/1945-7111/abfd73/meta
第一作者:Astrid F. Gunnarshaug
通訊作者:Signe Kjelstrup
通訊單位:挪威科技大學
編輯:jq
-
鋰電池
+關(guān)注
關(guān)注
260文章
8200瀏覽量
172110 -
電解質(zhì)
+關(guān)注
關(guān)注
6文章
821瀏覽量
20183 -
電池
+關(guān)注
關(guān)注
84文章
10706瀏覽量
131671
原文標題:鋰電綜述:電池中的可逆熱效應(yīng)及其計算方法
文章出處:【微信號:Recycle-Li-Battery,微信公眾號:鋰電聯(lián)盟會長】歡迎添加關(guān)注!文章轉(zhuǎn)載請注明出處。
發(fā)布評論請先 登錄
相關(guān)推薦
電阻器的工作原理與計算方法
波特率的定義和計算方法 波特率與數(shù)據(jù)傳輸速度的關(guān)系
石墨負極在鋰離子電池中的發(fā)展與儲鋰機制
電流計算方法與配線法的區(qū)別
電荷放大電路的帶寬 和IV轉(zhuǎn)換電路帶寬計算方法不一樣嗎?
使用位置傳感器輸出數(shù)據(jù)的角度計算方法

DCS系統(tǒng)I/O點數(shù)計算方法與原則
原電池中鹽橋的作用?
儲能容量的計算方法
電壓探頭延遲計算方法及應(yīng)用

原電池中鹽橋的三個作用是什么?
江西薩瑞微獨家研發(fā)【一種LDMOS場效應(yīng)管及其制備方法】





 探究電池中的可逆熱效應(yīng)及其計算方法
探究電池中的可逆熱效應(yīng)及其計算方法











評論