【研究背景】
鋰離子電池中除了電極,電解液也是電池中的重要組成部分。典型的液體電解質由混合溶劑、鋰鹽和添加劑組成,以上構成了經典的“溶劑化的陽離子”構型,并定義為Li+溶劑化結構(LSS),其會顯著影響離子電導率、離子遷移數和去溶劑化勢壘等電解質本征屬性,進而影響電池性能。傳統意義上,液體電解質的主要選擇標準包括高穩定性、與電極的兼容性、低粘度和低熔點。
在這些體系中,Li+通常被溶劑分子包圍,形成溶劑分離離子對(SSIP)結構。雖然其具備較好的流動性、解離程度及離子導電性,但仍會出現Li+的不均勻沉積和正極材料的溶解等問題,這和電解質的流動性及SSIP溶劑化結構密切相關,對其電解質調控,以實現LSS的調節至關重要。
【成果簡介】
近日,北京航空航天大學李彬助理教授團隊在ACS Energy Letters上發表題為“Solvation Structure-Tunable Phase Change Electrolyte for Stable Lithium Metal Batteries”的研究論文。作者通過篩選溶劑體系,最終確定以十二烷二酸二甲酯(DDCA)為溶劑制得一種物理固/液相變電解質(PCE),該PCE可通過物態變化調節Li+溶劑化結構(SSIP和CIP),進而實現鋰金屬負極的穩定運行,在不同溫度域下Li-LiMn2O4全電池均具備優異的庫侖效率和容量保持率。
【研究亮點】
(1)利用十二烷二酸二甲酯(DDCA)作溶劑,制得一種相變電解質(物態變化),具備離子電導率高、鋰離子遷移數大,及在固液相中均具備寬電化學窗口的特點。 (2)該相變電解質可通過改變其固/液物理狀態靈活可逆調節Li+溶劑化結構,可有效抑制鋰枝晶生長和正極Mn溶出。
【圖文導讀】
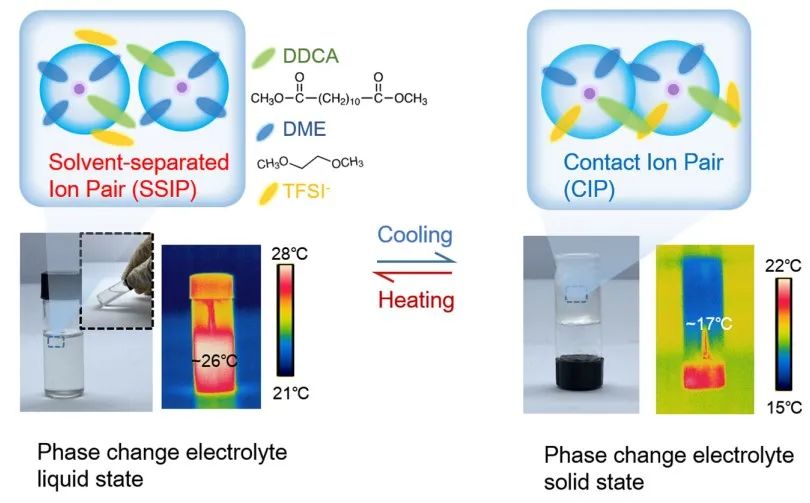
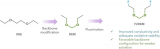
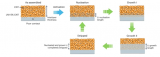
圖1 制備的PCE和相應的溶劑化結構示意圖。照片和紅外圖像顯示了PCE在固體和液體狀態下的物理狀態和溫度。上面的方框顯示了兩種狀態下對應的溶劑化結構. 作者篩選了一系列熔點相對較高的溶劑體系(>10 ℃),以DDCA為溶劑的體系展現了優異的性能,得到的電解液(PCE)體系(1.3 M LiTFSI DDCA:DME = 3:1 vol %),在22°C的熔點處具有相變特征 (液體/固體物態變化),如圖1所示。
利用拉曼光譜和分子動力學(MD)模擬,根據PCE的物理狀態的變化,發現LSS也可以在SSIP和CIP之間轉換,LSS的物態轉化有助于調節Li+傳導機制,并具有相對較高的離子導電性,即使在固體狀態下,也可獲得9.6 × 10?4 S cm?1的離子電導率。
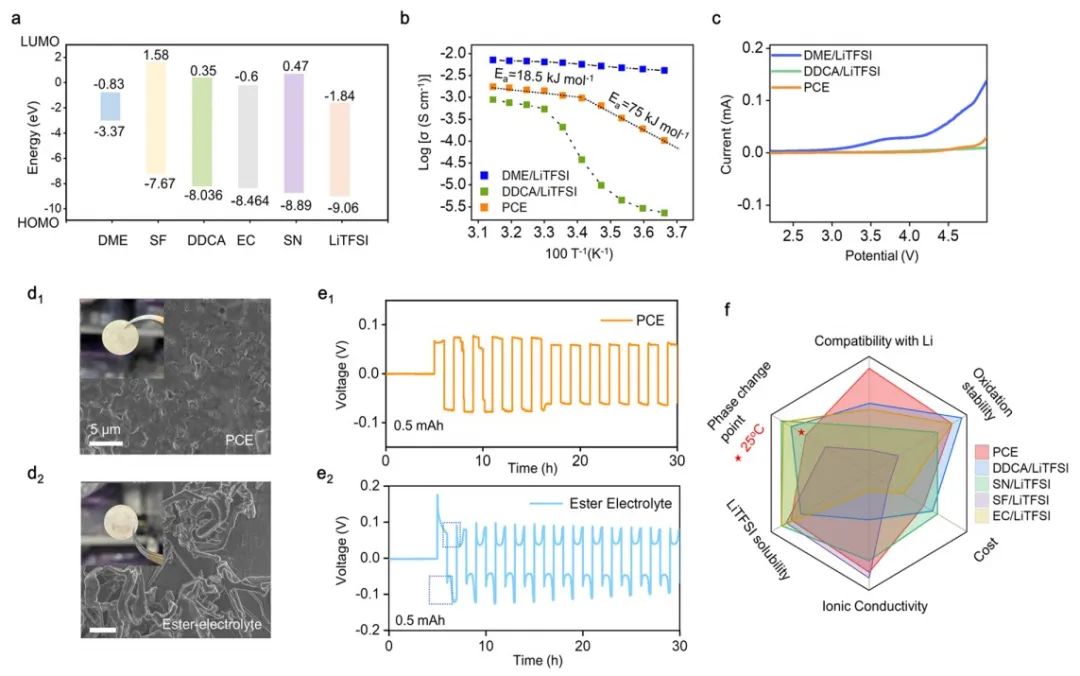
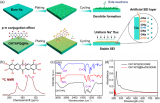
圖2 PCE的表征。(a) PCE和DDCA-LiTFSI、DME-LiTFSI的離子電導率在0 ~ 45℃之間的溫度相關性。(b)所選溶劑在相變點接近室溫時的HOMO/LUMO能級。(c)掃速為1 mV s?1時所選樣品的LSV曲線。(d) PCE-L (d1)和酯基電解質(d2)中鋰生長形態的SEM圖。(e)對稱電池在所選電解質中的循環,0.5 mA cm?2, 1 h。(f)雷達圖為所選相變電解質的評價標準。
如圖2a所示,DDCA、EC和SN的HOMO相對較低,具有較高的抗氧性。引入DME略微降低了抗氧化電位(4.75 V,圖2c),同時顯著提高了離子導電性,達到兩個數量級。如圖2b所示,在相變點附近,PCE的離子電導率在20 ℃時為9.6 × 10?4 S cm?1,在25℃時為1.11 × 10?3 S cm?1。
在~ 20°C的拐點處,轉折變化明顯。沉積的Li在PCE中呈光滑致密的形貌,如圖2d1所示。在酯基電解質中則呈典型的枝晶狀形貌,如圖2d2所示。鋰的形態演變也可以反映在鋰電池的極化曲線上,PCE的電壓分布是平坦的(圖2e1),說明鋰的沉積均勻循環過程中,枝晶的反復形成和生長導致液體電解質中電壓分布的顯著轉變和大量死鋰,如圖2e2所示。
因此,PCE不僅在所選的高熔點溶劑中表現出較好的綜合性能,而且在調節鋰沉積方面也優于液體醚和酯基電解質,如圖2f所概括。
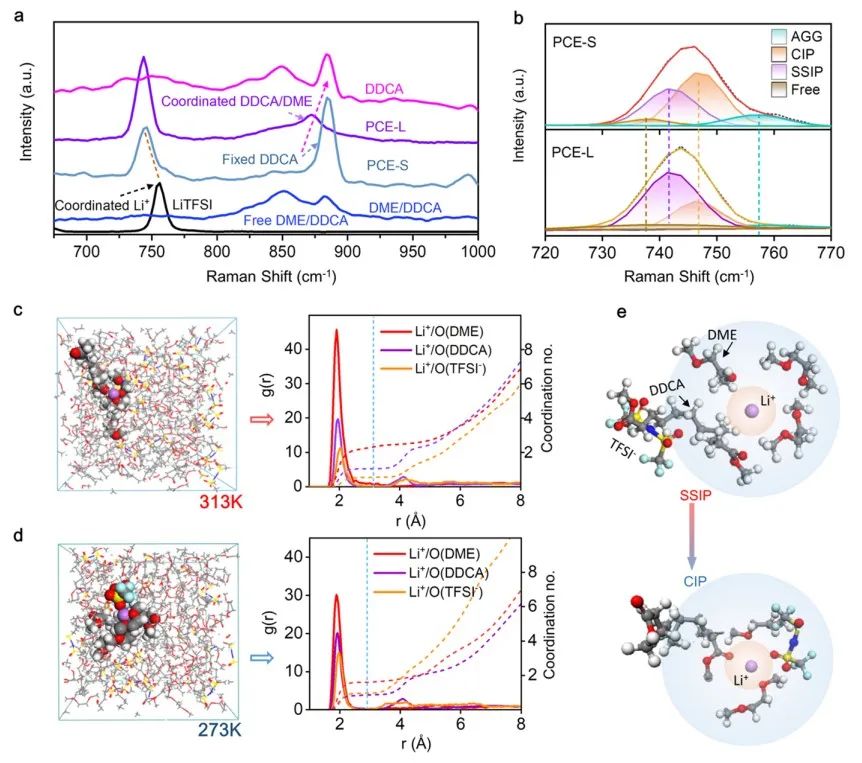
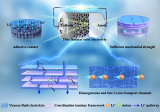
圖3 液態和固態PCE中溶劑化結構的演化。(a)研究對象的拉曼光譜。(b)液相和固相中TFSI?配位的拉曼擬合結果。(c, d)中間態(左)、RDF和配位數(右)分別從273和313 K的MD模擬中獲得。(x軸表示距離,左邊y軸表示分子的局部密度與圍繞中心分子r的距離處的體密度之比)。(e)從SSIP到CIP的溶劑化結構變化示意圖。
離子傳導能力與LSS密切相關,通過測量純DDCA、LiTFSI、DME/DDCA溶劑、液相PCE(PCE-l)和固態PCE(PCE-s)五種樣品的拉曼信號,確定了Li+中心的配位環境。如圖3a所示,在結晶LiTFSI中,位于約755 cm?1處的峰值歸因于TFSI?的特征伸縮振動峰。
在PCE-L中,這個峰經歷了一個紅移到743 cm?1,表明TFSI?和Li+之間的相互作用減弱了,其中溶劑分子在Li+中心周圍取代了TFSI?。同時,DME/DDCA溶劑的信號峰在PCE-L中有850~872 cm?1的藍移,證實了DME/DDCA溶劑分子與Li+的配位。
在PCE-S中,884 cm?1處的獨特峰信號代表了靜態DDCA分子的散射模型。圖3b進一步凸顯了顯示了TFSI?特征峰振動模式信號。 為了更深入地了解PCE的LSS,利用MD模擬分析了Li+在兩相狀態下的局部配位結構。在兩種溫度(313和283 K)下的平衡電解質軌跡如圖3c所示。計算得到相應的徑向分布函數(RDF)和配位數如圖3d所示。Raman和MD結果表明,LSS經歷了一個從液態的SSIP主導逐漸轉變為固態的CIPP主導的過程(圖3e)。
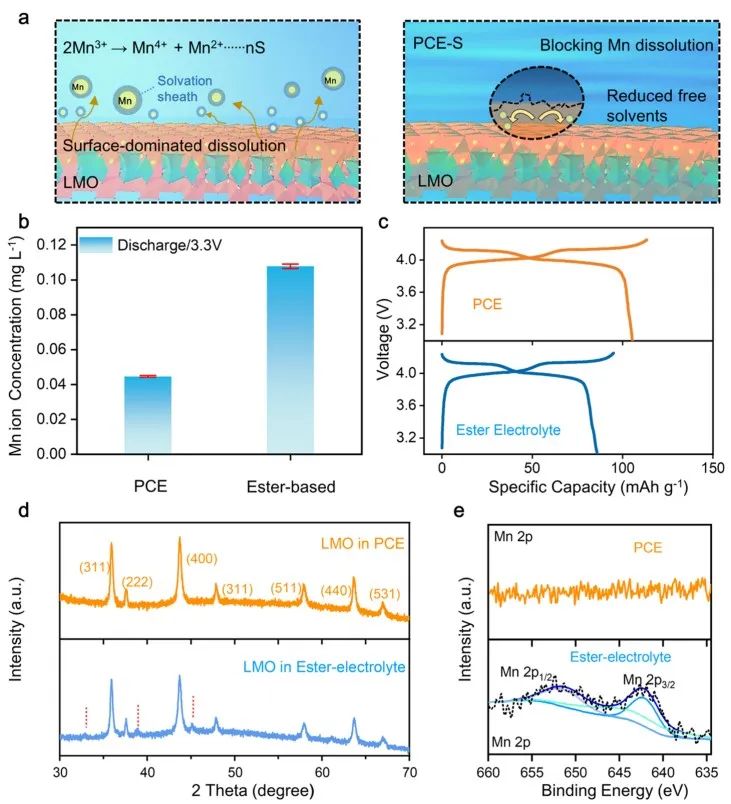
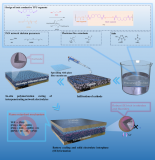
圖4 抑制正極Mn離子在PCE中的溶解。(a)酯基電解質(左)和PCE-s(右)之間不同的Mn離子溶解行為示意圖。(b) PCE-S和酯基電解質中的Mn離子濃度的ICP-OES結果。(c) PCE-S和酯基電解質中充放電曲線。(d) 20次循環后,LMO結構變化的XRD圖。(e) PCE和酯基電解質中鋰負極的XPS分析。
相變點以下的PCE具有固相和CIP結構,其特點是局部高濃度鹽,溶劑不易接觸,形成了一個天然的物理屏障,限制了金屬離子的溶解(圖4a)。在圖4b中,在3.3 V/15°C下放電一段時間后,PCE中檢測到的Mn離子濃度為酯基電解質的1/3。之后將放電的正極拆解并重新組裝,測試剩余容量和庫侖效率(CE)。
如圖4c所示,PCE中低溫放電后的剩余容量和CE分別為105 mAh g?1和93%。相比之下,在酯基電解質中,相應的值僅為85.4 mAh g?1和90.5%。 如圖4d所示,收集到的正極材料出現了LiMn2O4特征峰,證實了尖晶石結構。對于酯基電解質中的正極材料,在32.9°、38.8°和45.1°出現了新的明顯的峰,表明其存在大量Mn離子溶解。
在循環30次后,對Cu/Li負極進行XPS測試(圖4e)。Mn的信號峰只存在于有酯基電解質的電池中,這表明Mn離子的溶解行為不受限制。以上特征直接證明PCE-S在物理上阻斷了Mn離子的溶解,保持了LMO正極的結構完整性。
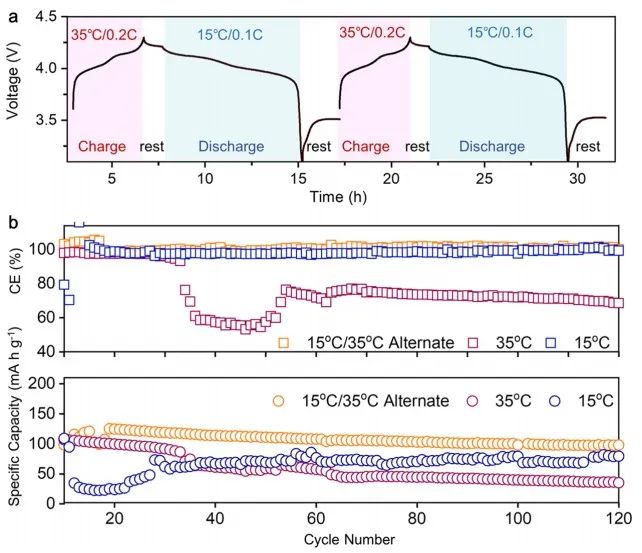
圖5 交替溫度條件下,Li-LMO電池的電化學性能。(a)充放電模式示意圖。(b) LMO-Li電池在PCE中的庫侖效率(上)和循環性能(下),分別采用溫度交替循環35℃和15℃。 實驗結果表明,錳離子在放電過程中損失更為嚴重。為了解決這一問題并提高LMO正極的穩定性,作者采用了一種新的交替溫度循環工步,巧妙利用了相變特性的優勢(圖5a)。
這種溫度交替工步綜合考慮了PCE-S在15℃時的離子電導率、Li沉積進而能量消耗,溫度過低或過高都會導致不必要的容量損失和能源浪費。為了進行比較,電池也在35或15°C的恒定溫度下循環。從圖5b中可以看出,溫度交替循環電池性能更為優異。
因此,交替溫度循環方案賦予了PCE在阻斷Mn離子溶解(放電過程中)和調節鋰沉積(充電過程中)方面的優勢,實現了長期循環穩定性。
【總結和展望】
作者通過簡單地調節由LiTFSI鋰鹽和DDCA和DME混合共溶劑組成的PCE的外部溫度和物態,實現了LSS的有效調控。研究發現根據PCE的物理狀態,LSS可以在SSIP和CIP之間進行轉化,LSS的原位轉化使PCE即使在固態狀態下也具有很高的離子導電性。
此外,與廣泛使用的液體電解質(酯和醚電解質)相比,PCE在調節鋰離子沉積和抑制正極Mn溶解方面表現出額外的優勢,特別是在不同溫度下。基于PCE獨特的性質,作者提出了交替溫度循環方案(15°C充電/35°C放電),Li-LMO電池的性能優于傳統的液體酯和醚電解質。
審核編輯:劉清
-
鋰離子電池
+關注
關注
85文章
3355瀏覽量
78883 -
電解質
+關注
關注
6文章
821瀏覽量
20695 -
LSS
+關注
關注
0文章
8瀏覽量
2076
原文標題:北航李彬ACS Energy Lett.:相變電解質助力高穩定性鋰金屬電池
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
超聲波焊接有利于解決固態電池的枝晶問題
清華大學:自由空間對硫化物固態電解質表面及內部裂紋處鋰沉積行為的影響
研究論文::乙烯碳酸酯助力聚合物電解質升級,提升高電壓鋰金屬電池性能

固態鋰電池最新突破
通過電荷分離型共價有機框架實現對鋰金屬電池固態電解質界面的精準調控





 相變電解質助力高穩定性鋰金屬電池
相變電解質助力高穩定性鋰金屬電池















評論