目前,全球范圍內出現的新型冠狀病毒(SARS-CoV-2)不同變體和其他與病毒相關的威脅令人擔憂,特別是病毒獲得的突變增強了其傳播力,影響了診斷和疫苗效力。因此,迫切需要開發快速、準確和易于使用的病毒診斷/檢測方法。另一方面,當一種新的未知病原體或新的突變出現時,找到合適的受體進行檢測是至關重要的,特別是對于無標記傳感系統。而理想的無標記傳感系統除了需要對與傳感器表面結合的材料特性變化具有高敏感性之外,還必須能夠通過適當的表面功能化和受體來確保檢測的特異性。
然而,獲得針對新目標的生物識別元素涉及到一個獲得高質量特定材料的多步驟過程。而該過程通常只能獲得極少量的產物(低濃度和小體積)。因此,新的檢測平臺除了需要具備高靈敏度之外,還應高度小型化,以允許利用微量樣品進行多次檢測。
據麥姆斯咨詢報道,近期,來自波蘭華沙理工大學(Warsaw University of Technology)等機構的研究人員介紹了一種基于光纖誘導的微腔串聯馬赫-曾德爾干涉儀(μIMZI)的實時、高度小型化傳感方案,可用于SARS-CoV-2之類病毒顆粒檢測。該檢測方法旨在檢測體積小至數百皮升的樣品中SARS-CoV-2病毒顆粒的保守區域,其檢測限可以達到ng/mL水平。相關研究成果以“Low-volume label-free SARS-CoV-2 detection with the microcavity-based optical fiber sensor”為題發表于Scientific Reports期刊。
如圖1所示,這項工作首次利用基于微腔的光纖傳感器直接檢測SARS-CoV-2病毒顆粒。考慮到病毒的不斷進化,該研究應用的生物傳感方法是基于抗核衣殼SARS-CoV-2蛋白抗體。N蛋白是病毒核衣殼的主要組成部分,通過與病毒RNA結合決定復制周期。
利用蛋白N作為靶點最重要的依據是,根據臨床研究報告,該蛋白在感染早期會大量表達;此外,與翻譯后修飾較多的S蛋白相比,N蛋白在Ser176位點只有一個特征較好的o-磷酸化位點,且沒有糖基化位點。因此,與受體的結合親和力不會受到干擾,使N蛋白成為SARS-CoV-2感染早期診斷靶點的理想候選者。
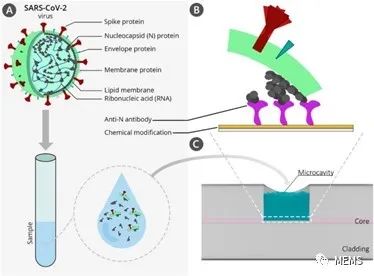
圖1 基于微腔的光纖傳感器檢測SARS-CoV-2之類病毒顆粒示意圖
與其他的無標記生物傳感裝置相比,該研究基于定制化的且可獲得量(體積和濃度)小的非商用生物材料【即SARS-CoV-2病毒顆粒、抗N蛋白(特別是SARS-CoV-2的重組N蛋白RNA結合域)抗體】,因此需要微量傳感系統。所提出的傳感器有助于測量皮升體積的樣品,并實現生物分子相互作用的無標記和實時監測。因此,它可以在不超過30分鐘的時間內完成一步式檢測。此外,通過對傳感器表面進行化學官能化優化,可以實現ng/mL范圍內的出色靈敏度水平。
研究人員制造的傳感器形狀和直徑如圖2A所示。為了在表面化學修飾和生物測定之前對μIMZI傳感器進行表征,在微加工過程之后對其RI靈敏度進行了測量。如圖2B所示,隨著RI的增加,發射功率和最小波長都發生了變化。在圖2C中,繪制了最小波長與RI的對應關系。
每個樣本對應的點用最小二乘法線性逼近,以確定特定RI區域的靈敏度。結果顯示,該工作所提出的μIMZI在較短波長(綠色線表示)和較長波長(藍色線表示)的RI靈敏度分別達到10000 nm/RIU以上和14000 nm/RIU以上(圖2C)。
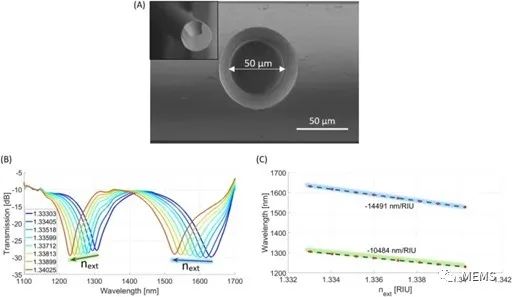
圖2 微腔串聯馬赫-曾德爾干涉儀(μIMZI)傳感器SEM圖像及靈敏度表征
隨后,為了驗證該傳感方法的有效性,研究人員將利用μIMZI檢測的結果與利用標準化技術(如ELISA)所獲得的結果進行了比較。結果顯示,μIMZI檢測靈敏度水平優于ELISA。此外,靈敏度水平與現有的無試劑側向流動檢測相當,其檢測限在ng/mL范圍。
然而,需要指出的是,鑒于每個病毒顆粒的蛋白質拷貝數很大(~ 1000),μIMZI傳感器已被設計用于檢測/靶向核衣殼蛋白。而COVID-19陽性患者的常見病毒載量在每毫升10?-10?個病毒之間,因此感染期間的N-蛋白水平明顯高于傳感器的檢測限。唾液中的N-蛋白水平在COVID-19感染初期為數十pg/mL,在接下來的幾天內甚至可以達到數百ng/mL。
在血液中,N-蛋白濃度比唾液中的小,但差異不大,能夠維持在數十至數百pg/mL的水平。因此,可以得出結論,μIMZI甚至可以用于診斷低病毒載量的無癥狀病例。
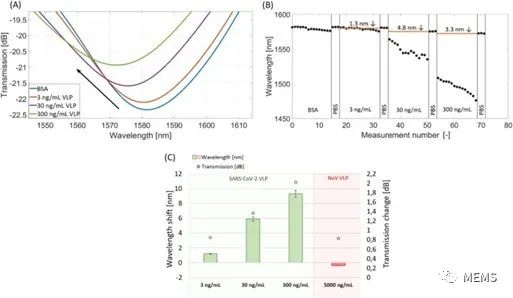
圖3 微腔串聯馬赫-曾德爾干涉儀(μIMZI)在實驗的每個階段對用作受體的抗N抗體和不同濃度的SARS-CoV-2之類病毒顆粒的響應
綜上所述,該研究報道了第一個用于病毒檢測的基于微腔的光纖傳感器。該傳感技術可以快速、直接、無標記、特異性和高靈敏度地檢測所選靶標。該傳感器實時檢測SARS-CoV-2之類病毒顆粒的最低檢測限為ng/mL。需要強調的是,該傳感器只需pL級體積樣品即可正常工作。
因此,除了檢測外,該微腔串聯馬赫-曾德爾干涉儀(μIMZI)還可以用于研究、分析和驗證低濃度/低體積受體與所選靶標之間的相互作用。這些反過來又對基礎研究、藥物發現和開發新的傳感平臺至關重要,尤其是在疫情爆發,并出現了如SARS-CoV-2等新病原體的時候。
審核編輯:劉清
-
傳感器
+關注
關注
2564文章
52665瀏覽量
764185 -
光纖傳感器
+關注
關注
16文章
323瀏覽量
35247 -
傳感系統
+關注
關注
1文章
95瀏覽量
17088 -
RNA
+關注
關注
0文章
46瀏覽量
9885
原文標題:利用基于微腔的光纖傳感器實現微量無標記新冠病毒檢測
文章出處:【微信號:MEMSensor,微信公眾號:MEMS】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
光纖傳感器應用領域 光纖傳感器工作原理
光纖光柵傳感器:精準測量與監測的科技先鋒
光纖傳感器在工業中的應用
光纖傳感器比傳統傳感器強在哪?——以大壩監測為例

利用光纖間接檢測 X 射線





 利用光纖傳感器實現微量無標記新冠病毒檢測
利用光纖傳感器實現微量無標記新冠病毒檢測












評論