隨著能源需求的增長和環保要求的提升,市場對高效可充電電池儲能系統的需求日益迫切,尤其是在太陽能和風能等可再生能源存儲領域。鋰離子電池(LIBs)以其高工作電壓、高比能量、便攜性、良好的低溫性能和長壽命等優勢,被認為是最佳候選之一。然而,電池中使用液態電解質導致了電解液泄漏、起火和爆炸等問題,限制了其長期發展。此外,在電化學過程中產生的中間產物可能會溶解在有機電解質中,導致傳統LIBs的庫侖效率(CE)降低。還有鋰枝晶生長問題發生在陽極,伴隨著有機電解質中發生的副反應。此外,液態電解質的有限電壓窗口難以與鋰陽極和新開發的高電壓陰極材料相協調。根本的解決方案是用無機固態電解質(SSE)取代有機液態電解質,組裝具有高安全性、高可回收性和廣泛應用范圍的固態鋰離子電池(SSLBs)。
鑒于此,深圳清華大學研究院(清華深研院)劉思捷/香港科技大學KristiaanNeyts教授團隊在《AdvancedEnergy Materials》國際期刊上綜述研究了硫化物/聚合物復合固態電解質及其全固態鋰離子電池的應用。
為了實現相應SSLB的高能量密度,SSE必須滿足幾個條件:
(i) 電解質的厚度應該薄且壓實。與液態電解質相比,SSLBs通常展現出更高的密度有效提高SSLBs的能量密度需要減少電解質的厚度,這有助于在電池結構內更高效地利用空間。
(ii) 電解質和電極的結構需要穩定,并在充放電循環過程中保持接觸。提高整體相位的結構穩定性可以避免由于晶格畸變引起的顆粒破裂,從而中斷與固態電解質的物理接觸。同時,SSE需要具有出色的柔韌性、塑性,并且高度壓實,以解決SSLBs的界面問題。此外,電極與SSE之間的界面復雜多樣,應根據不同電極材料的特性選擇合適的SSE系統,并構建穩定的界面。
(iii) 必須有一個連續的傳導通道網絡。在SSB的SSE中構建離子遷移通道。在這種情況下,隨著電池循環的演變,電極的固-固界面組成變得更加復雜。在陰極顆粒上涂覆或原位形成快速離子導體層對Li+傳輸是有益的。
如上所述,上述三種主流SSE各有優缺點,導致單一類型的SSE無法滿足所有條件。因此,結合兩種或三種SSE優點的固體復合電解質(SCEs),具有很大的優勢,這可能是提高SSLBs性能的可行方法(如圖1)。
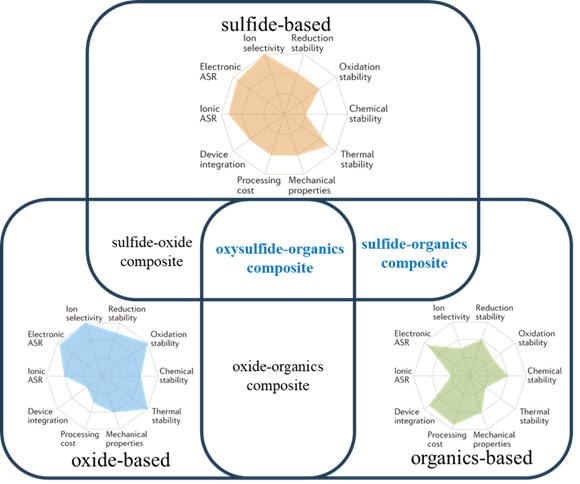
SSEs的性能屬性和分類圖的雷達圖。ASR。
硫化物-聚合物復合固態電解質(SSEs)的制備方法
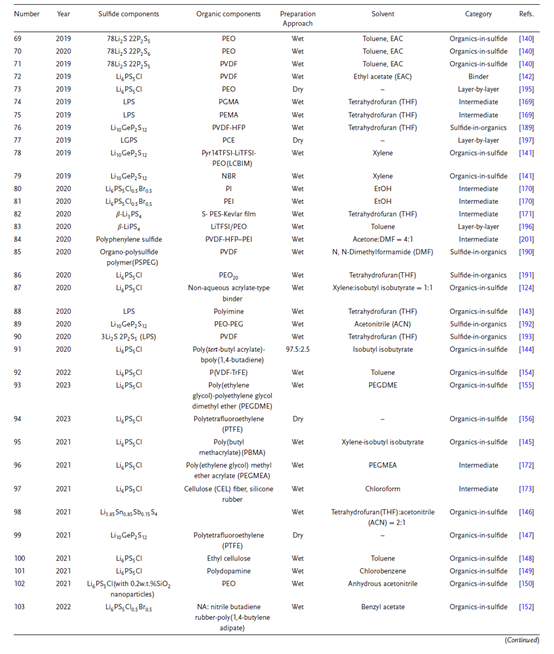
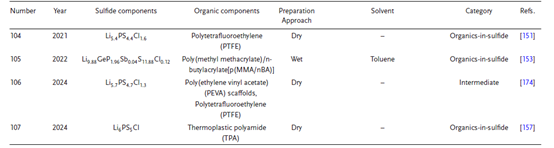
硫化物-聚合物復合固態電解質(SSEs)的制備方法是將硫化物和有機組分混合在一起,然后干燥復合電解質膜或片。通常有兩種類型:干法和濕法,如圖20所示。干法是將硫化物電解質粉末與有機電解質粉末混合,不添加任何液體添加劑,然后進行相應的實驗,如高溫固態反應、機械化學方法和熔融淬火方法。濕法是采用有機溶劑或室溫下為液態的聚合物電解質,然后將硫化物電解質和聚合物電解質在液態介質中混合進行后續實驗。需要注意的是,由于硫化物對空氣中的濕度敏感,硫化物-有機復合SSEs的合成需要在惰性氣氛中進行。表5提供了硫化物-有機復合SSEs制備方法的詳細總結。
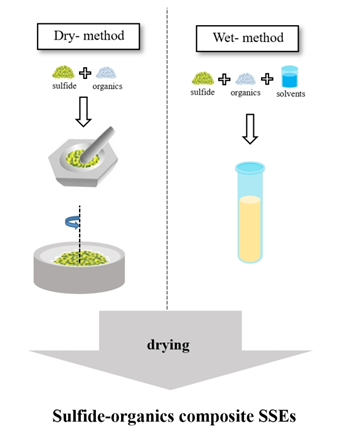
硫化物-有機物復合SSEs的制備方法。
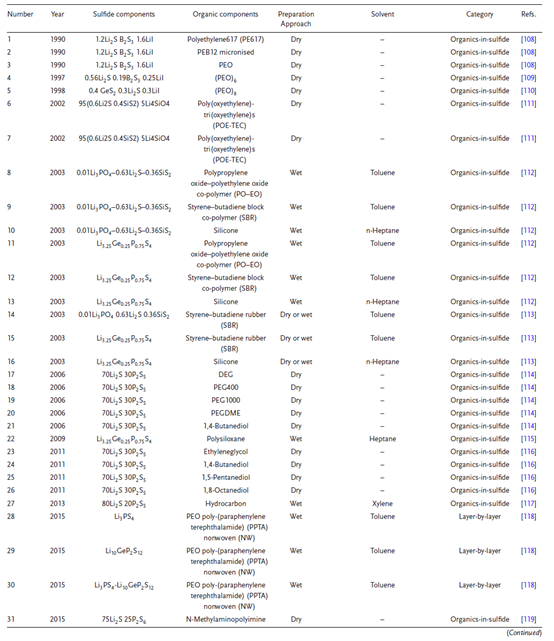
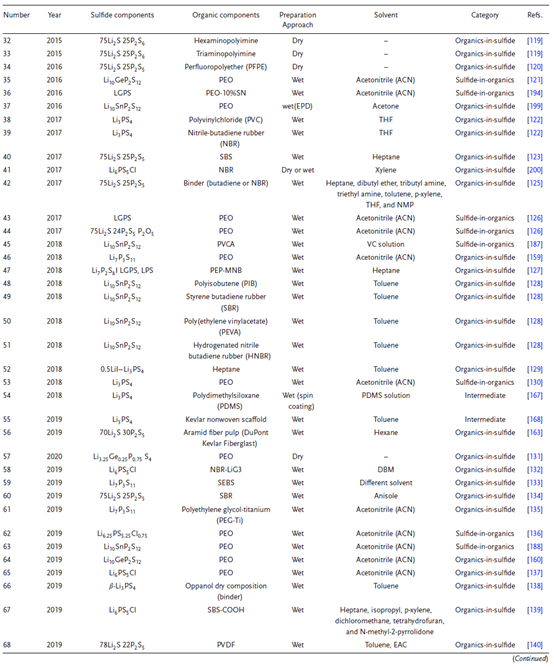
硫化物-有機物復合SSEs制備方法的總結表
硫化物聚合物復合SSE分類
硫化物-有機物復合 SSE 的分類根據硫化物-有機物復合SSE中硫化物與有機物的比率,有四種類型的硫化物-有機物復合 SSE:“硫化物-有機物”(具有較高硫化物/有機物質量比的復合 SSE)、“即時”(具有相當有機物和硫化物含量的復合 SSE)、“有機物中硫化物”(具有較高有機物/硫化物質量比的復合 SSE)和“逐層”(圖 1)。
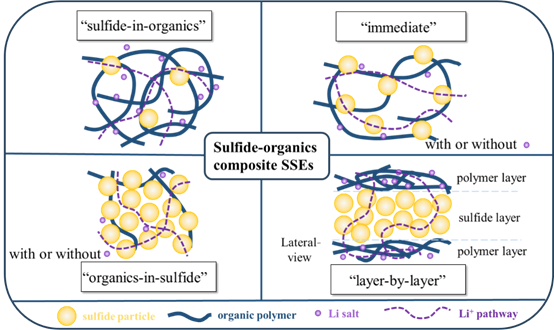
硫化物-有機物復合 SSE 的示意圖
盡管硫化物 SSE 具有最高的離子電導率,但其發展受到與負極和正極電極的易界面反應的阻礙。在 SSB 中,硫化物 SSE 是鋰離子導體,而氧化物陰極是最常用的商業陰極材料是混合離子電子導體(MIEC),它具有特別高的電子導電性。因為氧和鋰之間的鍵合比硫和鋰之間的鍵合強得多,所以鋰在氧化物和硫化物之間的電化學電位必須有很大的不同。這表明氧化物陰極和硫化物 SSE 之間存在化學勢差,當鋰離子緊密接觸時,它們會從硫化物 SSE 移動到陰極以達到平衡并形成空間電荷層。鋰離子的遷移產生空位和間隙離子,這兩者都有助于離子傳導。但 Ohta 等人的研究觀察發現LCO和Li3.25Ge0.25P0.75S4(硫代-LISICON)之間的空間電荷層的高電阻導致SSB倍率性能不佳。因此,了解和改進陰極/硫化物 SSE 的界面以改善當前 SSB 的電化學性能非常重要。
Organics-in-Sulfide SSE
有機物作為機械增強和 Li+ 導電路徑
在復合電解質中,硫化物顆粒在很大程度上負責鋰離子的傳輸,可能伴隨著硫化物顆粒的碎裂。值得一提的是,硫化物和有機物之間的界面也占鋰電導貢獻的很大一部分,而聚合物-鋰鹽由于其低離子電導率,對鋰離子的傳輸貢獻了一小部分。因此,在這種情況下,有機物用作機械增強和 Li+ 導電路徑。同時,有機物的加入可以在保持相對較高的離子電導率的同時減小復合電解質的厚度,從而實現相應 SSLBs 的高能量密度。
有機物作為粘合劑
由于敏感的硫化物很容易與有機化合物反應產生不良產物,因此選擇合適的有機物作為粘合劑非常重要。Inada等人比較了兩種硫化物電解質(0.01Li3PO4-0.63Li2S-0.36SiS2、Li3.25Ge0.25P0.75S4)與不同有機粘合劑(PO-EO、SBR和硅膠)的復合SSEs性能。在每種情況下,有機硅復合材料的導電性都比其他復合材料高得多。有機硅是一種可交聯的液體單體,它是液體,在加熱前將被擠壓到復合 SSE 顆粒中被壓縮的硫化物顆粒之間的空隙中。液態硅氧烷在雜化電解質內部形成顆粒狀結構域,加熱后仍能保持質構,通過快速交聯反應將液態硅氧烷變為固體硅橡膠。因此,硫化物顆粒之間的離子電導率不受強烈影響。
更高分子量的粘合劑可以增強 SSE 薄膜的結構完整性;然而,它們也會導致晶界電阻增加和臨界電流密度降低。相反,低分子量聚合物(例如聚(異丁烯))薄膜雖然分布更均勻,但缺乏與活性材料持續接觸所需的應變硬化或強度。最值得注意的是,使用較高分子量粘合劑的 ASSB 表現出更好的放電容量保持能力,這與在使用較低分子量粘合劑的細胞中觀察到的顯著容量下降形成鮮明對比。
immediate 復合SSE
當有機物含量和硫化物含量相等時,可以形成中間復合 SSE(圖 2b)。如上所述,當有機物含量極低時,它構成有機物硫化物復合 SSE。其中,當加入鋰鹽時,有機物可以充當鋰離子傳輸通道,增強電解質的機械性能。當沒有鋰時,有機物可以作為粘合劑,填充硫化物顆粒中的間隙,使電解質更加緊湊。由于有機物本身的絕緣性,復合 SSE 的電導率通常隨著有機物含量的增加而降低,因為有機物可能會覆蓋硫化物顆粒之間的鋰傳導路徑。但是,當一些有機化合物具有特殊結構(如網絡、導線等)時,可以使用一定量的有機化合物作為支撐復合 SSE 的骨架/框架,以獲得良好的彈性和鋰離子滲透性雜化膜。
總之,通過有機-無機共價鍵、有機物本身的網狀結構、靜電紡絲等實驗方法制備了具有網絡結構的有機化合物電解質,然后加入幾乎等量的硫化物電解質。最終可以獲得過渡型中間復合 SSE。這種類型的 SSE 要么通過有機物-無機鍵合提供更多的鋰導電位點,要么由于有機化合物的網絡結構,支撐整個復合 SSE,有機物不會完全屏蔽硫化物顆粒之間的鋰導電路徑,可以保證膜的柔韌性。
Sulfide-in-Polymer Composite 復合SSEs
聚合物 SSE,一直受到其低離子電導率的限制(最常用的 PEO 基聚合物電解質的離子電導率在室溫下約為~10 -7 S?cm-1),這主要是由于室溫下聚合物體系中的結晶度高和少量無定形型造成的。另一個問題是界面穩定性差,電極表面容易形成鈍化膜。結果,鋰離子在沉積和溶解過程中電流分布不均勻,產生枝晶,影響電池的循環性能和電流密度。為此,研究人員嘗試了各種方案來提高其離子電導率。經過研究人員 20 多年的努力,從最初的純固體聚合物電解質到摻雜無機納米顆粒的復合聚合物電解質,室溫電導率比原始聚合物基 SSE 提高了 4 個數量級或更多,處于實際應用水平之內。
從(圖2c)中可以看出,制備的混合固體電解質膜是半透明的和有彈性的。混合 SSE 表面的FESEM圖像顯示,沒有觀察到裸露的顆粒。填料均勻嵌入PEO聚合物中,并覆蓋有完整的PEO聚合物。雜化SSE膜表面沒有明顯的多孔結構(圖2d-2e)。與惰性填料相比,添加活性填料可以進一步提高離子電導率。PEO@1%SiO2和 PEO@20%SiO2 在室溫下的電導率分別為 5.4×10-6S?cm-1 和 9.7×10-7S?cm-1。在活性填料中,只需 1% 的硫化物(LGPS, LPOS)即可達到與 20% 的氧化物填料(LAGP)相同的電導率水平(圖2f-2g)。
干法
由于硫化物容易與有機溶劑發生化學反應,最初研究的最直接方法就是在干燥環境中將硫化物電解質和聚合物電解質粉末混合。之后,燒結后的硫化物粉末直接與聚合物粉末混合。為了使硫化物和聚合物的混合物更加均勻和顆粒化,球磨被廣泛使用。
總的來說,固相法是制備復合電解質的一種相對簡單的方法。首先,可以通過簡單的混合和研磨來制備。其次,可以通過球磨進行更精確的混合,并且可以發生機械化學反應,在硫化物和有機物之間創建化學鍵。球磨等制造方法有助于有效混合并為離子傳導創造協同界面。
濕法
對于硫化物-有機復合SSEs的溶液/漿料,最實用的方法是濕法。具體來說,將硫化物電解質和聚合物電解質加入溶液中攪拌均勻,或者如果聚合物本身在室溫下為液態,則將硫化物電解質加入聚合物液體中攪拌。混合均勻后,干燥成固態,材料可以壓制成片;或者材料可以干燥成漿料,然后涂覆在支撐體上。
由于硫化物容易與有機溶劑反應,因此必須仔細選擇合適的溶劑進行復合SSEs的液相合成。研究人員通常在采用液相方法制備復合電解質之前,會比較不同溶劑對所研究的硫化物電解質的影響,或者根據先前研究的結果選擇合適的溶劑。Tan等人使用不同溶劑對Li7P3S11進行分散,以測試溶劑對電解質的影響(圖21a)。
目前濕法合成也已被用于一些新的實驗合成方法,如電泳沉積(EPD)和旋涂。Blanga等人使用以丙酮為基的沉積浴的低成本方法制備LSPS@PEI復合膜。Pang等人通過旋涂將稀釋的PDMS溶液和固化劑滲入β-Li3PS4層,得到一種有彈性且鋰離子滲透的混合膜。
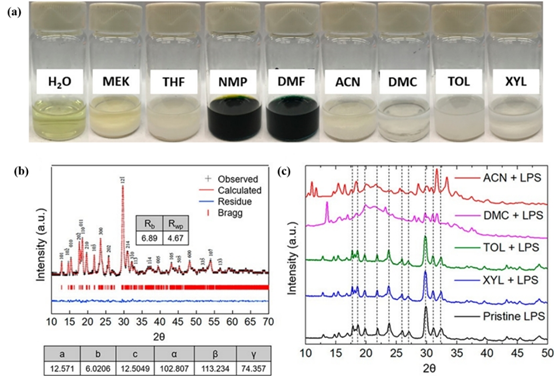
(a) Li7P3S11添加后不同溶劑的顏色變化;(b) 原始Li7P3S11的Rietveld精修;(c) Li7P3S11在CAN、DCM、TOL和XYL中分散后的XRD圖譜,(a)-(c) 轉載自參考文獻,經許可。版權所有2018,美國化學會。
干法與濕法的比較
2003年,Inada等人研究了硫化物-有機復合SSEs的制備方法,包括干法和濕法,其中涉及苯乙烯-丁二烯共聚物(SBR)或硅橡膠(硅膠)作為聚合物粘合劑。通過原始干法合成的硫化物-有機復合SSEs通常具有更高的導電性。雖然干法在改善材料性能和潛在的創新電解質設計方面提供了顯著優勢,但它也面臨著與擴大規模生產相關的挑戰。這些挑戰通常源于對專用設備的需求和增加的勞動力需求。相比之下,濕法受益于已建立的流程和現有的生產線,使其更具成本效益,適合大規模制造。然而,由于溶劑使用和額外的后處理步驟,它可能涉及更高的材料成本。盡管如此,濕法可以作為生產實際電池所需的大型和薄型固體電解質片的有效方法之一,盡管由于更均勻的混合和一些溶劑與硫化物之間的反應,它有絕緣有機網絡屏蔽鋰路徑的缺點。通過選擇合適的溶劑和聚合物,可以通過液相方法獲得高離子導電性的復合電解質。總體而言,兩種方法都有各自的優缺點。雖然干法是技術開發中的一個有前景的前沿領域,但在實現完全工業化之前仍有一段距離。短期內,由于已建立的流程和現有基礎設施,濕法在大規模生產方面提供了更大的實用性和可行性。然而,從長遠來看,干法在該領域也具有重要的發展潛力和創新前景。
物理化學穩定性
硫化物-有機復合固態電解質膜的機械穩定性對于電池在封裝和充放電循環過程中承受應力至關重要,同時也影響著電極與電解質之間的附著力。硫化物固態電解質通常具有脆性,顆粒中存在約15%的孔隙率,通過用有機聚合物填充這些空隙可以提供額外的機械強度。這種改進在一定程度上源于聚合物的柔韌性,同時也因為填充硫化物SSE的孔隙使電解質密度更高,從而降低其開裂的可能性。例如,由80%的75Li2S·25P2S5和20%的聚酰胺組成的復合電解質膜的理論和幾何密度顯示,聚酰胺的柔韌性和填充孔隙的特性使其相對密度約為0.97,表明微結構中無空隙。通過線性流變測量研究了75Li2S·25P2S5@PFPT復合電解質在30℃下的儲能(G')和損耗(G")剪切模量頻率(ω)的依賴性,結果顯示復合電解質具有彈性固體特性,G"遠大于G',且兩者均與頻率無關,剪切模量為2.6 MPa,比原始75Li2S·25P2S5(5.9 GPa)低三個數量級,顯著提高電解質的粘附性能和柔韌性。
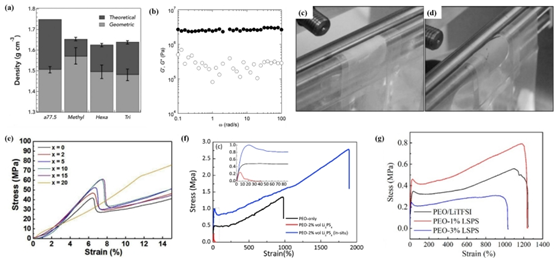
(a) 由80%75Li2S·25P2S5和20%聚酰胺組成的SEPM膜的理論和幾何密度;(b) 復合電解質的線性流變測量。在30℃下測量的復合電解質的存儲模量和損耗模量的頻率依賴性;(c) 帶有2.5% HNBR;(d) 10% SBR的熱軋SE薄膜的管狀帶測試;(e) 不同PEO含量電解質顆粒的應力-應變曲線;(f) 不同制備電解質的應力-應變曲線;(g) 各種聚合物電解質膜的拉伸強度。
空氣穩定性
硫化物固態電解質通常與空氣中的氧和水蒸氣發生不可逆的化學反應,導致結構改變和離子電導率降低,嚴重制約了其在固態鋰電池中的應用。與此同時,聚合物SSE在空氣中具有較好的穩定性,因此,硫化物-有機復合SSE被認為是緩解硫化物電解質在空氣中不穩定性的解決方案之一。Tan等人研究了Li7P3S11與不同聚合物結合的空氣穩定性復合電解質,發現不同聚合物的疏水性可以通過測量其與水的接觸角來比較,其中SEBS是最疏水的聚合物,其接觸角為103°。通過在潮濕空氣中產生H2S來檢測復合電解質的空氣穩定性,結果表明復合電解質中的疏水SEBS可以顯著提高膜在空氣中的水分穩定性,與裸Li7P3S11粉末相比,相對降低50-55%。在復合電解質中加入5 wt.%或10 wt.%的SEBS后,可以觀察到,在相同暴露條件下,與Li7P3S11裸樣品相比,H2S的產量明顯減少。更引人注目的是,原始的Li7P3S11在與水接觸時完全溶解,而復合電解質膜在完全浸入水中時保持完整。這一結果表明,疏水聚合物的使用有助于水敏Li7P3S11電解質在潮濕空氣中的穩定。
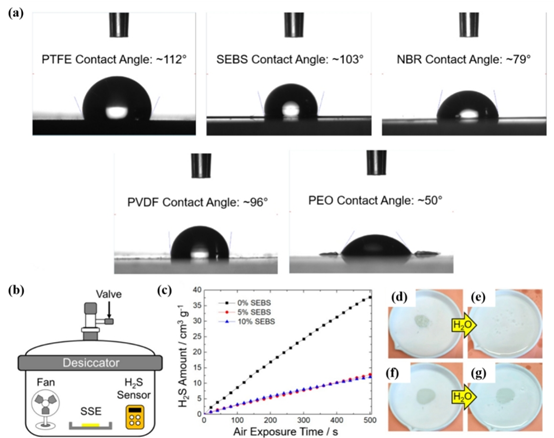
(a) SEBS、NBR、PVDF、PEO與水的接觸角,表示每種聚合物的疏水性;(b)用于測量空氣中100mg Li7P3S11水解時H2S氣體的裝置;(c)固定體積空氣中暴露于100 mg裸Li7P3S11和100 mg疏水性SEBS聚合物復合材料時H2S釋放量與時間的關系;(d)-(e)浸水前后Li7P3S11裸態;(f)-(g)復合電解質膜浸水前后。
電化學穩定性窗口
電解液的電化學穩定性是提高固態鋰電池能量密度的重要因素。為了研究復合膜的電化學穩定窗口,大多數相關工作采用線性掃描伏安法(LSV)和電流電壓法(CV)測量。硫化物SSE的發展受到電化學穩定窗口狹窄的限制,通過有機聚合物的加入可以在一定程度上穩定和擴大這一窗口。Li等組裝的SSLi7P3S11@PEG-Ti/Li電池在-0.2 ~ 9.5 V (vs. Li+/Li)范圍內的CV曲線顯示,電解液和金屬鋰在高達9.5 V時具有良好的穩定性,如此寬的電化學窗口表明其具有良好的實際應用價值。具有寬電化學窗口的L-P-S玻璃體系SSE還可以通過添加PEO電解質消除CV曲線的波動,使電解質/鋰界面更加穩定。
對于有機聚合物SSE,電化學窗口一般比硫化物SSE寬,但對于某些特定應用,電化學電解質需要加寬(例如用于高壓氧化物陰極)。一些研究表明,在有機聚合物中加入硫化物活性顆粒可以略微增加電化學窗口和穩定性。Li等人使用Li6.25PS5.25Cl0.75作為PEO SSE的有源填料,并進行了LSV測試,PEO@1wt% Li6.25PS5.25Cl0.75、PEO@3wt% Li6.25PS5.25Cl0.75、PEO和PEO@5wt% Li6.25PS5.25Cl0.75分別在5.1V、4.0 V、3.8 V和3.0 V以下均未記錄到明顯電流。在所有硫化物SSE中,Li10GeP2S12相的分解電位可超過5 V,因此常將LGPS作為活性填料添加到有機化合物中,以達到擴大電化學窗口的目的。添加少量硫化物填料可以拓寬有機聚合物的電化學穩定性窗口,原因有三:首先,硫化物顆粒表面的- sh鍵具有促進TFSI-與硫化物顆粒成鍵的功能,使陰離子流動性降低。由于鹽陰離子的不可逆氧化反應導致陽極不穩定窗口,因此硫化物顆粒與鹽陰離子之間的氫鍵可以有效地阻止陰離子被氧化分解。其次,添加硫化物顆粒的復合電解質具有更高的離子電導率,減少了鋰離子在電極與電解質界面附近的積累,從而降低了界面過電位,提高了電極與電解質的相容性。第三,可以選擇一些電化學窗口相對較寬的單離子導體無機填料,如LGPS。與那些復雜的制備工藝和高成本的方法相比,它是一種簡便、經濟的方法。但是,由于大多數硫化物電解質(如L-P-S玻璃和LPSCl)的電化學窗口狹窄,添加過多的硫化物活性顆粒會降低這種強烈的效果。
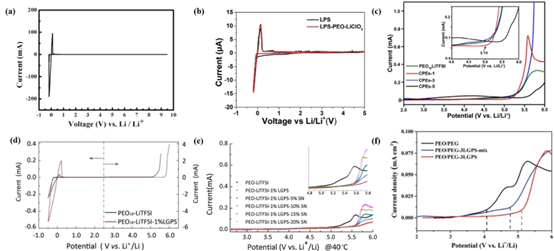
(a) SS/LPS-200-PT-2-Li-24/Li電池CV曲線;(b)鋰/LPS/不銹鋼電池和鋰/LPS- peo - liclo4 /不銹鋼電池的CV ;(c)掃描速率為0.25 mV/s,溫度為60℃時LSV曲線的電化學穩定窗口;(d) 80℃時聚合物電解質的LSV和CV曲線;(e) 40℃時LSV曲線的電化學穩定窗口;(f)室溫下各電解質的LSV曲線。
鋰金屬負極的電化學穩定性
金屬鋰電極與硫化物-有機物復合SSE在SSLB中的界面穩定性對電池的循環壽命和倍率性能起著重要作用。為了研究鋰和硫化物-有機復合SSE之間的穩定性,在各種工作中對對稱Li/sulfide@organics/Li電池進行了測試。Zhang等研究的對稱Li/Li6PS5Cl@x%PEO/Li電池在電流密度為0.3 mA·cm?2時的電壓分布圖顯示,原始Li6PS5Cl的電壓曲線在830小時后過電位逐漸升高,而不同PEO含量的電池在1200小時內電壓分布保持較低。結果表明,在Li6PS5Cl中加入PEO可以增強鋰的穩定性,該復合電解質適合與鋰陽極配對。在Li等人的工作中,Li/PGMA@LPS50%/Li電池的電壓曲線呈現出平緩穩定的電鍍和剝離曲線,在1mA·cm?2下,其過電位在100 h內為~ 500 mV。相比之下,以純LPS為電解質的對稱鋰電池顯示出約800 mV的大且不穩定的過電位。當電流密度為0.5mA·cm?2時,PGMA@LPS50%的對稱電池在約340次循環中具有穩定的極化,電壓穩定在300 mV左右。結果表明,在硫化物SSE中加入有機聚合物可以增強其抗鋰穩定性,復合SSE適合與鋰陽極配對。在逐層硫化物-有機復合SSE中,有機聚合物被設計為硫化物和鋰金屬之間的中間層。經過50次循環后,Li/LGPS/Li的過電位為750 mV,而Li/PCE-LGPS-PCE/Li的過電位在0.13 mA·cm-2下在250 h內保持在40 mV。相關表征也證實了有機界面層的加入可以抑制金屬Li對硫化物的還原或分解,抑制枝晶的生長。
硫化物聚合物復合SSEs在鋰電池中的應用
硫化物-有機物復合SSEs因其高離子電導率、寬電化學窗口、良好的界面接觸和有效抑制鋰枝晶的優點,在固體鋰電池中得到了廣泛的應用。典型的鋰金屬電池近年來,基于硫化物-有機物復合SSEs的SSLBs越來越受到關注,并提出了各種創新的電池設計方案,旨在盡快將SSLBs轉化為實際應用。由于硫化物-有機物復合SSEs具有增強的氧化穩定性,即更寬的電化學穩定性窗口,因此它們適合與高壓陰極材料(如LiNixCoyMn1?x?yO2, LiCoO2 and LiMn2O4)匹配,以實現高能量密度SSLBs。例如,Oh 等人所采用的 Li6PS5Cl @NBR-LiG3的LiNi0.6Co0.2Mn0.2O2電極在 30°C 時呈現出高達174 mA? h? g -1的高容量。
LiNi0.7Co0.15Mn0.15O2電極的高面容量達 7.4 mA? h? cm-2,其超高質量負載為45 mg? cm-2。β-Li3PS4@Oppanol復合物與聚乙二醇(PEO)的層狀結構 SSE 被 Ates 等人(如圖 26a 至 26e 所示)涂覆于 Li1+x[Ni0.6Mn0.2Co0.2]1-xO2復合陰極上或用作自支撐帶,展現出良好的循環性能和特定容量(約 140mAh/g)。
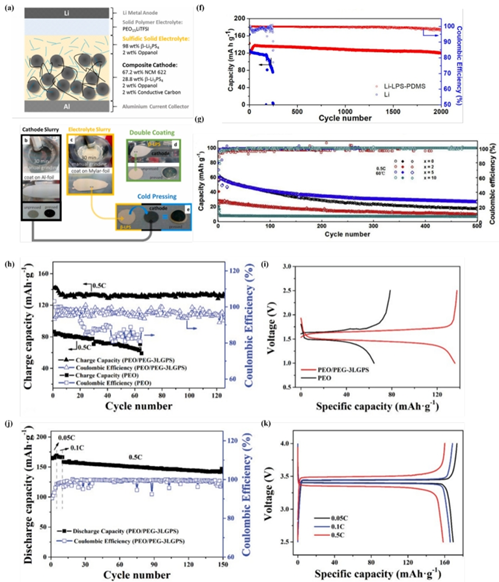
(a)雙電解質層電池的示意圖;(b)陰極和(c)通過漿料涂覆生產電解質帶;(d)-(e)陰極電解質的冷壓。
鋰硫電池
硫和硫化合物被認為具有作為陰極活性材料的巨大潛力,因為它們具有較高的理論比容量(例如,S的1672 mA?h?g-1,Li2S的1166 mA? h? g -1),通常與鋰金屬陽極結合組裝鋰硫電池。盡管鋰硫電池因其高能量密度和功率密度可以滿足未來動力電池市場的需求,但不幸的是,傳統的鋰硫電池具有嚴重的穿梭效應,其中反應中間體多硫化鋰溶解在電解質中,從而增加了電解質的粘度并降低了離子電導率。此外,多硫化鋰可以在陰極和陽極之間不斷移動,并在陽極表面被還原為硫化鋰,導致活性物質的損失。為了解決這個問題,建議硫化物C有機物復合SSEs的應用應有效消除穿梭效應,并引起更多關注,如Li等人在圖(a)-27(c)中所示。他們組裝了一個S/LGPS@PEO/Li鋰電池在0.2℃和0.5℃下分別以1183 mA? h? g-1和719 mA? h? g-1表現出優異的倍率性能,并在0.1℃下完成了50次循環,容量保持率為588 mA? h? g-1。有機復合SSEs中的硫化物也用于Li-S電池,據報道,Li-S電池由以下成分組成:PEO@1wt%Li10SnP2S12電解質具有優異的電化學性能、高放電容量(1000 1000 mA? h?g-1 )、高庫侖效率和60℃下的良好循環穩定性(圖27d-27e)197。最重要的是,PEO@1wt%Li10SnP2S12電池具有吸引人的性能,具有高比容量(800 mA? h?g-1)和即使在50℃下也具有良好的循環穩定性,而基于PEO的Li-S電池由于PEO電解質的低離子電導率和高界面電阻材料的高理論比容量(例如,S的1672mA? h? g-1,Li2S的1166 mA? h? g-1)而無法成功放電,通常與Li金屬陽極結合組裝Li-S電池。盡管鋰硫電池因其高能量密度和功率密度可以滿足未來動力電池市場的需求,但不幸的是,傳統的鋰硫電池具有嚴重的穿梭效應,其中反應中間體多硫化物鋰溶解在電解質中,從而增加了電解質的粘度并降低了離子電導率。此外,多硫化鋰可以在陰極和陽極之間不斷移動,并在陽極表面被還原為硫化鋰,導致活性物質的損失。為了解決這個問題,建議硫化物-有機物復合SSEs的應用應有效消除穿梭效應并引起更多關注。
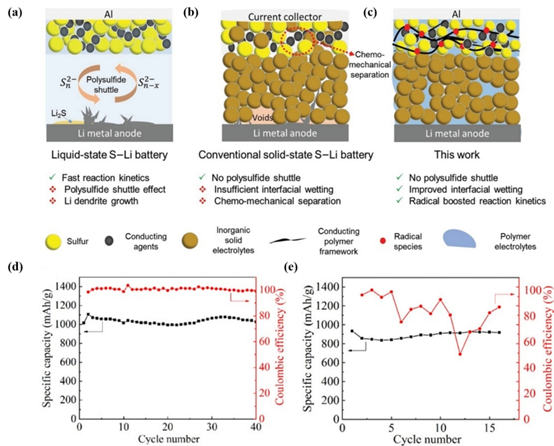
(a)液體S-Li電池單元,(b)傳統固態S-Li電池單體,(c)固態S-Li蓄電池單體135的構造(d) PEO-1% LSPS電解質和PEO/LiTFSI電解質在(e)
總結
本文重點介紹了應用于SSLBs的硫化物-有機物復合SSEs的研究與開發。從廣義上講,對于具有單個組件的SSEs來說,很難滿足商業應用的需求。另一方面,硫化物-有機物復合SSEs可以繼承硫化物和有機SSEs的優點,與純聚合物SSEs相比,表現出更高的離子電導率、更優的熱穩定性和電化學穩定性,以及與原始硫化物SSEs相比更好的柔韌性和更低的界面電阻。隨著復合電解質中硫化物與有機物的比例逐漸增加,復合電解質從有機物中的硫化物轉變為直接硫化物,然后轉變為硫化物型有機物。特別地,可以通過交錯硫化物和有機SSEs來形成逐層類型。在硫化物SSEs中的有機物中,有機物可以作為粘合劑(不含Li鹽)或作為機械增強和Li導電路徑(含Li鹽或使用極性聚合物)。有機物可以填充硫化物SSEs中的間隙,使電解質更緊湊、更有彈性。在即時的SSEs中,具有三維網絡結構的有機物質可以作為骨架貫穿整個電解質,使復合電解質成為柔性和可彎曲的超薄膜。在有機硫化物SSEs中,具有超高離子電導率的硫化物活性填料可以改變聚合物基質的鏈結構,降低聚合物的結晶度,從而提高離子電導率。對于逐層類型,通過在硫化物SSEs和電極之間引入聚合物中間層,可以在保持高離子電導率的同時大大提高電解質和電極的界面不穩定性。目前,一些典型的鋰金屬電池和鋰硫電池已經采用硫化物C有機物復合SSEs作為電解質。硫化物-有機物復合SSEs具有高離子電導率、良好的機械強度、界面潤濕性、良好的熱穩定性和電化學穩定性等突出特點,在各種鋰電池系統中表現良好。綜上所述,復合SSEs的設計和制備,聚合物電解質和無機電解質的和諧結合,實現各組分的功能雜化,已成為提高SSEs性能的有效途徑。硫化有機復合SSEs可以結合兩種SSEs的優點,提高SSLBs的性能。通過精確控制復合固體電解質的組成和結構,可以控制其機械性能、離子電導率、界面穩定性和其他物理和化學性能。與此同時,硫化物-有機物復合SSEs的研究引起了人們對影響復合電解質電化學性能的機理的興趣,新的相關工作也在不斷涌現。然而,硫化物-有機物復合SSEs體系仍然很難達到高離子電導率和鋰離子遷移數、良好界面穩定性和強力學性能的基本要求。對于實際應用,硫化物-有機物復合SSEs仍有許多問題需要解決。
展望
盡管硫化物-有機物復合SSEs在高溫或室溫下的電導率可達10-3~10-4S?cm-1,但仍低于液體電解質的電導率(10 -2 S?cm-1),不足以滿足許多實際應用。因此,硫化物-有機物復合SSEs的電導率應進一步提高。硫化物-有機物復合SSEs體系室溫電導率和界面穩定性的增強機制尚不完全清楚。只有少數研究論文研究了硫化物-有機物復合材料SSEs的鋰導電機理。硫化物-有機物復合SSEs的電化學性能有待進一步提高,這需要進一步研究增強機理。
通常,對于硫化物SSEs中的有機物,向硫化物SSEs添加有機物會降低電解質的離子電導率。換句話說,通過犧牲一部分良好的離子導電性,可以獲得優異的界面穩定性、機械性能和低厚度,硫化物電解質的靈敏度將與大多數有機化合物反應。因此,有必要開發不與硫化物反應并能保持SSEs離子導電性的新型有機化合物。有必要進一步優化改性硫化物活性顆粒的物理和化學性質,如納米粒子、小粒徑、表面引入多個基團,以提高硫化物在有機SSEs中的離子電導率以及SSEs與電極的界面穩定性。進一步研究硫化物-有機物復合固體電解質中各組分的協同作用和界面性質,將為提高復合固體電解質的性能提供指導。
硫化物-有機物復合SSEs的合成工藝需要進一步優化,這是邁向實用、大規模SSLBs的重要一步。這種優化至關重要,原因有幾個。首先,可擴展的合成方法對于大規模生產中一致的質量和性能至關重要,因為目前的技術通常只能生產有限數量的高質量復合材料。此外,改進這些工藝可以降低生產成本,使SSLBs與傳統鋰離子電池更具競爭力。提高SSEs的電化學性能在很大程度上取決于它們的微觀結構、離子電導率和機械性能。優化的合成可以帶來更好的離子傳輸和更好的循環穩定性。此外,電解質和電極之間界面相容性的改善可以最大限度地減少電阻和降低性能的副反應。優化策略包括控制合成條件、選擇合適的前體、實施合成后處理以及采用自動化、高通量技術。通過關注這些領域,我們可以推進硫化物-有機復合SSEs的發展,并將其整合到實用的大規模SSLBs中。
深圳清華大學研究院低碳能源與節能技術重點實驗室副主任、副研究員,香港科技大學助理研究員(合作)劉思捷為論文第一作者及通訊作者。其他主要貢獻者為先進顯示與光電子技術國家重點實驗室主任,香港科技大學教授Kristiaan Neyts;香港科技大學助理研究員周樂;中國農業大學鐘廷珺;中山大學吳鑫副教授。研究得到深圳市可持續發展專項項目的資助。
-
鋰離子電池
+關注
關注
85文章
3341瀏覽量
78802 -
太陽能
+關注
關注
37文章
3518瀏覽量
115738 -
電解質
+關注
關注
6文章
821瀏覽量
20659
原文標題:清華深研院劉思捷/港科大Kristiaan Neyts最新AEM:硫化物/聚合物復合固態電解質助力高比能全固態鋰離子電池發展
文章出處:【微信號:清新電源,微信公眾號:清新電源】歡迎添加關注!文章轉載請注明出處。
發布評論請先 登錄
聚合物固態電解質的合理設計
關于全固態鋰金屬電池的高性能硫化物電解質?
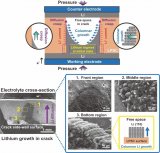
清華大學:自由空間對硫化物固態電解質表面及內部裂紋處鋰沉積行為的影響





 硫化物/聚合物復合固態電解質及其全固態鋰離子電池的應用
硫化物/聚合物復合固態電解質及其全固態鋰離子電池的應用











評論